-
반응공학 - 평행반응과 연속반응화공기사 필기/반응공학 2021. 3. 17. 14:53
1. 첫번째 평행 반응
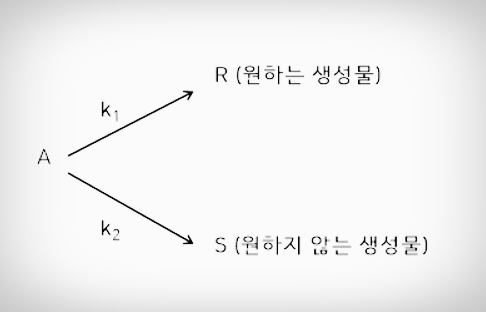
첫번째 평행 반응 위의 평행반응에서의 R과 S에 대한 반응속도식은 다음과 같다.

R과 S에 대한 반응속도식 여기서 R과 S의 상대적인 생성속도의 비를 구하고 그 비를 가능한 크게 하려고 한다. 이렇게 함으로써 어떤 반응기를 써야 효과적이며 원하는 생성물(R)을 얻기 위해서 어떻게 해야 하는 지 알 수 있다.

R과 S의 상대적인 생성속도의 비 1) a1 > a2 일때 (원하는 반응 > 원하지 않는 반응)
- 선택도 R/S의 비를 높이기 위해선 반응물의 농도가 높아져야 한다. R을 생성하기 위해서는 회분반응기나 플러그 흐름 반응기(PFR)이 효율적이다.
2) a1 < a2 일때 (원하는 반응 < 원하지 않는 반응)
- 원하는 반응이 원하지 않는 반응보다 반응차수가 낮은 경우 R을 생성하기 위해서는 반응물의 농도가 낮아야 한다. 따라서 큰 혼합흐름 반응기(CSTR)을 사용해야 한다.
3) a1 = a2 일때
- 두 반응의 반응차수가 같으므로 rR/rS = k1/k2 = 상수 이다. 따라서 반응기의 유형에는 무관하며 반응차수의 비 k1/k2에 의해 결정된다.
cf. k1/k2를 변화시키는 방법
① 운전 온도를 변화시키는 방법
② 촉매를 사용하는 방법
4) 농도 조절
① Ca를 높게 유지하는 방법
- 회분식 반응기, 플러그 흐름 반응기(PFR)사용
- Xa(전화율)을 낮게 유지
- 공급물에서 불활성 물질을 제거
- 기상계에서 압력을 증가
② Ca를 낮게 유지하는 방법
- 혼합흐름 반응기(CSTR) 사용
- Xa(전화율)을 높게 유지
- 공급물에서 불활성 물질을 증가
- 기상계에서 압력을 감소
2. 두번째 평행 반응

두번째 평행 반응 위의 평행반응에서의 R과 S의 반응속도비는 다음과 같다.

R과 S의 반응속도비 a1,a2,b1,b2의 크기 대소에 따라 나눠보면 다음과 같다.
1) a1 > a2, b1 > b2 일때
- Ca↑, Cb↑
- Batch, PFR, 직렬로 연결된 CSTR 사용
- 기상계에서 고압
- A와 B를 한번에 넣음
2) a1 < a2, b1 < b2 일때
- Ca↓, Cb↓
- 큰 CSTR 에 A, B를 천천히 혼힙
- 기상계에서 저압
- 불활성 물질을 넣음
3) a1 > a2, b1 < b2 일때
- Ca↑, Cb↓
- 많은 양의 A에 B를 천천히 넣음
4) a1 < a2, b1 > b2 일때
- Ca↓, Cb↑
- 많은 양의 B에 A를 천천히 넣음
3. 비가역 연속 1차 반응

비가역 연속 1차 반응 비가역 연속 반응의 반응속도는 다음과 같이 나타낼 수 있다.

비가역 연속 반응의 반응속도 비가역 연속 반응에서 중간체의 최고 농도와 그때의 시간을 PFR, CSTR 반응기로 각각 구해보면 다음과 같다.
1) PFR

PFR일 때 증간체의 최고농도와 시간 2) CSTR

CSTR일 때 증간체의 최고농도와 시간 3) 성능의 특성
- 원하는 생성물(R)의 최대농도를 얻는데 있어서 k1 = k2 인 경우를 제외하고는 항상 PFR이 CSTR보다 짧은 시간을 요구한다. ( 이 시간차는 k2/k1이 1에서 멀어질수록 점점 커진다.)
- PFR에서의 R의 수율이 CSTR에서 보다 항상 크다
- k2/k1 ≪ 1 이면 A의 전화율을 높게 설계해야 하며, 이때 미사용 반응물의 회수는 필요없다.
- k2/k1 > 1 이면 A의 전화율을 낮게 설계해야 하며, R의 분리와 미사용 반응물의 회수가 필요하다.≪
'화공기사 필기 > 반응공학' 카테고리의 다른 글
반응공학 - 온도와 압력의 영향 (0) 2021.03.18 반응공학 - 수율 (0) 2021.03.17 반응공학 - 순환반응기 (0) 2021.03.16 반응공학 - 반응기의 크기 비교 (1) 2021.03.16 반응공학 - 흐름식 반응기(CSTR, PFR) (0) 2021.03.11